
Los científicos de la Universidad de Osaka en Japón han identificado una proteína que funciona como regulador maestro del envejecimiento celular, lo que podría abrir nuevas puertas para los tratamientos de reversión del envejecimiento. Esta proteína, conocida como AP2A1, parece controlar si las células se mantienen jóvenes o entran en senescencia, un estado en el que las células dejan de dividirse pero no mueren.
La investigación se centra en lo que les sucede a las células humanas durante el proceso de envejecimiento. A medida que las personas envejecen, sus cuerpos acumulan células "senescentes" que han dejado de dividirse. Estas células similares a zombis crecen anormalmente grandes, producen compuestos inflamatorios y contribuyen a numerosas enfermedades relacionadas con la edad, desde la artritis hasta la enfermedad de Alzheimer.
Relacionado: Si Eres Un Amante Del Vino Tinto ¡Tenemos Buenas Noticias!
Lo que hace que este descubrimiento sea particularmente notable es cómo la manipulación de solo esta proteína produjo resultados espectaculares. Cuando los investigadores redujeron los niveles de AP2A1 en las células senescentes, muchos marcadores del envejecimiento se revirtieron: las células se redujeron a un tamaño normal, comenzaron a dividirse nuevamente y mostraron otras características juveniles. Ocurrió lo contrario cuando aumentaron la AP2A1 en células jóvenes, lo que provocó que desarrollaran de forma prematura rasgos de envejecimiento.
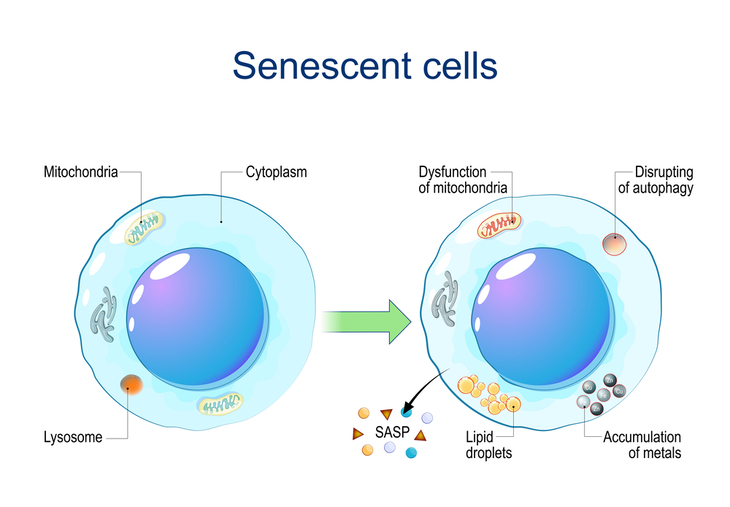
El envejecimiento celular no es un proceso aleatorio. En la década de 1960, el científico Leonard Hayflick descubrió que las células humanas solo pueden dividirse aproximadamente 50 veces antes de detenerse definitivamente, una limitación que ahora se conoce como el "límite de Hayflick". Esto representa un aspecto fundamental de cómo envejecen las células.
Cuando las células se vuelven senescentes, sufren transformaciones importantes. Pueden hincharse hasta seis veces su tamaño normal y desarrollar estructuras internas distintivas, en particular "fibras de estrés" gruesas, hebras de proteínas que se extienden a través de la célula como vigas de soporte. Las células senescentes también producen menos proteínas, se mueven más lentamente y expresan genes específicos asociados con el envejecimiento.
Los investigadores notaron que un aspecto desconcertante de las células senescentes es cómo mantienen su enorme tamaño. Las fibras de estrés inusualmente gruesas encontradas en las células envejecidas proporcionaron una pista importante que condujo a su descubrimiento.
El equipo japonés hizo su descubrimiento comparando fibroblastos de piel humana jóvenes (células que producen colágeno) con otros más viejos que se habían vuelto senescentes. Entre muchas diferencias, encontraron que las células senescentes contenían niveles mucho más altos de AP2A1.
La AP2A1 (subunidad de adaptina alfa 1 de la proteína adaptadora 2) funciona principalmente en la endocitosis mediada por clatrina, esencialmente el sistema de reciclaje de la célula para llevar materiales al interior. Hasta este estudio, nadie había relacionado esta proteína con el proceso de envejecimiento.
En sus experimentos más convincentes, los investigadores utilizaron la interferencia del ARN para reducir los niveles de AP2A1 en células viejas. Los resultados fueron sorprendentes: las células se volvieron más pequeñas, sus fibras de estrés se adelgazaron, reanudaron la división y mostraron una menor expresión de genes relacionados con el envejecimiento. Esencialmente, la reducción de AP2A1 rejuveneció las células.
En el experimento opuesto, el aumento de AP2A1 en células jóvenes provocó que desarrollaran características de envejecimiento: crecieron más, desarrollaron fibras de estrés más gruesas, desaceleraron su tasa de división y expresaron marcadores genéticos de senescencia.
Los investigadores descubrieron que AP2A1 regula cómo las células se adhieren a su entorno circundante. Las células se conectan a su entorno a través de estructuras llamadas adherencias focales que actúan como anclas. En las células senescentes, estas adherencias focales se vuelven anormalmente grandes y fuertes.
AP2A1 aparentemente ayuda a transportar una proteína llamada integrina β1 a lo largo de las fibras de estrés para construir y mantener estas adherencias focales agrandadas. El anclaje mejorado explica por qué las células senescentes mantienen su tamaño anormalmente grande.
El equipo de investigación confirmó que los niveles de AP2A1 aumentan en varios tipos de células senescentes, no solo en aquellas que llegan al final de su vida útil replicativa. Cuando expusieron células jóvenes a la radiación ultravioleta o a fármacos que inducen la senescencia, los niveles de AP2A1 aumentaron drásticamente, lo que sugiere que el aumento de esta proteína es una característica universal de la senescencia celular independientemente de la causa.

Este descubrimiento abre posibilidades apasionantes para la medicina antienvejecimiento. El desarrollo de fármacos que inhiban la AP2A1 o sus vías podría rejuvenecer las células senescentes del cuerpo, lo que podría ralentizar o incluso revertir aspectos del envejecimiento. Este enfoque podría ser valioso para tratar enfermedades relacionadas con la edad que se caracterizan por la acumulación de células senescentes, como la osteoartritis, las enfermedades cardiovasculares y los trastornos neurodegenerativos.
Los hallazgos, publicados en Cellular Signalling, van más allá de la simple comprensión del envejecimiento. Las células senescentes desempeñan funciones complejas en nuestros cuerpos: si bien contribuyen al envejecimiento y las enfermedades relacionadas, el proceso de senescencia también ayuda a prevenir el cáncer al detener la división de células potencialmente peligrosas. Cualquier intervención dirigida a las células senescentes debería equilibrar estas consideraciones cuidadosamente.
Relacionado: Te Brindamos Los Mejores Consejos Para Vivir Más Tiempo
Las aplicaciones de esta investigación podrían ir más allá de los tratamientos antienvejecimiento. Comprender cómo las células controlan su tamaño y forma podría ayudar a desarrollar nuevos enfoques para tratar enfermedades caracterizadas por un crecimiento celular anormal, como el cáncer. También podría proporcionar información sobre la cicatrización de heridas, donde los fibroblastos desempeñan papeles cruciales.
Como regulador clave de la senescencia y el rejuvenecimiento, AP2A1 ha sido identificado como un nuevo objetivo prometedor para promover la salud celular y la longevidad. Los investigadores identificaron a AP2A1 como un biomarcador valioso y un objetivo terapéutico potencial para el rejuvenecimiento celular.
En el complejo rompecabezas del envejecimiento, el descubrimiento del papel de AP2A1 representa un avance importante, que revela un punto de control central que coordina múltiples aspectos del envejecimiento celular. Al manipular esta proteína, los investigadores pueden haber encontrado una forma de indicar a las células si deben comportarse como jóvenes o como viejas, lo que esencialmente les otorga el poder de hacer retroceder el reloj celular.